
SUDOSCAN a prouvé son efficacité dans le domaine de la néphrologie.
La neuropathie autonome périphérique est le résultat d'une lésion des nerfs périphériques ou d'une neuropathie à petites fibres due à des nerfs myélinisés (type Aδ), ainsi qu'à des nerfs non myélinisés (fibres non myélinisées du groupe C). Dans la neuropathie périphérique, les petites fibres somatiques et autonomes peuvent être affectées. Ces petites fibres contrôlent la perception de la température, la perception de la douleur et le fonctionnement autonome, comme le système cardiaque, pulmonaire et entérique. [1].
La neuropathie périphérique peut être une complication de plusieurs maladies, notamment le diabète, les problèmes neurologiques ou métaboliques et les infections.
La neuropathie diabétique peut se manifester chez les personnes qui en sont aux premiers stades du diabète. Sudoscan permet de dépister précocement les symptômes microvasculaires, ce qui aide les médecins à mieux soigner leurs patients et à prévenir les complications graves.
Le Sudoscan peut également aider à évaluer les patients aux stades avancés de la maladie, qui risquent de développer des complications graves liées à leur maladie (telles que l'hypotension intradialytique ou la neuropathie cardiaque autonome).
1 - SUDOSCAN détecte les personnes à haut risque de néphropathie diabétique [2].
Contexte : L'étude évalue l'efficacité du Sudoscan (®) pour détecter la néphropathie diabétique (DKD) chez les patients chinois atteints de diabète de type 2. Compte tenu du lien entre la dysglycémie, la vasculopathie et la neuropathie, une identification précoce de la néphropathie diabétique est cruciale.
Méthodologie : Le Sudoscan a été mesuré sur 50 patients atteints de diabète de type 2 ne présentant pas de DKD et sur 50 patients diabétiques de type 2 présentant une DKD. Une analyse statistique a été réalisée pour établir une corrélation entre la mesure du Sudoscan et les indicateurs de la fonction rénale afin de déterminer sa sensibilité et sa spécificité dans la détection de la maladie de DKD.
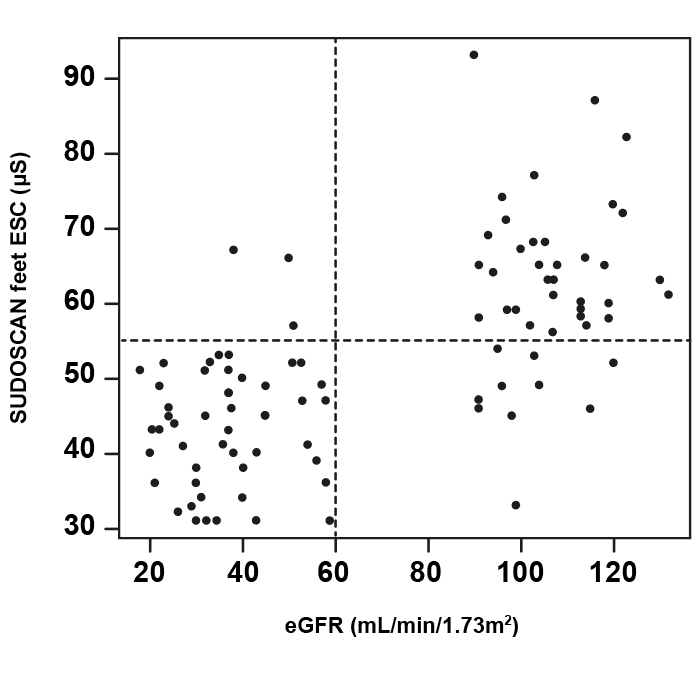
Résultats : Les mesures du Sudoscan étaient étroitement liées aux indicateurs de la fonction rénale et de l'albuminurie. Une mesure Sudoscan inférieure à 55 a montré un taux élevé de sensibilité (94%) et une spécificité de 78% pour la détection de la maladie de DKD. En outre, après ajustement pour d'autres facteurs de risque, le Sudoscan a pu être associé de manière indépendante à la maladie coronarienne. Les patients ayant une faible mesure de Sudoscan sans DKD avaient une période de maladie plus longue et étaient plus susceptibles de souffrir de complications associées au diabète.
2 - SUDOSCAN peut être utilisé pour évaluer le risque d'hypotension intradialytique (IDH) chez les patients en hémodialyse (HD) [3]
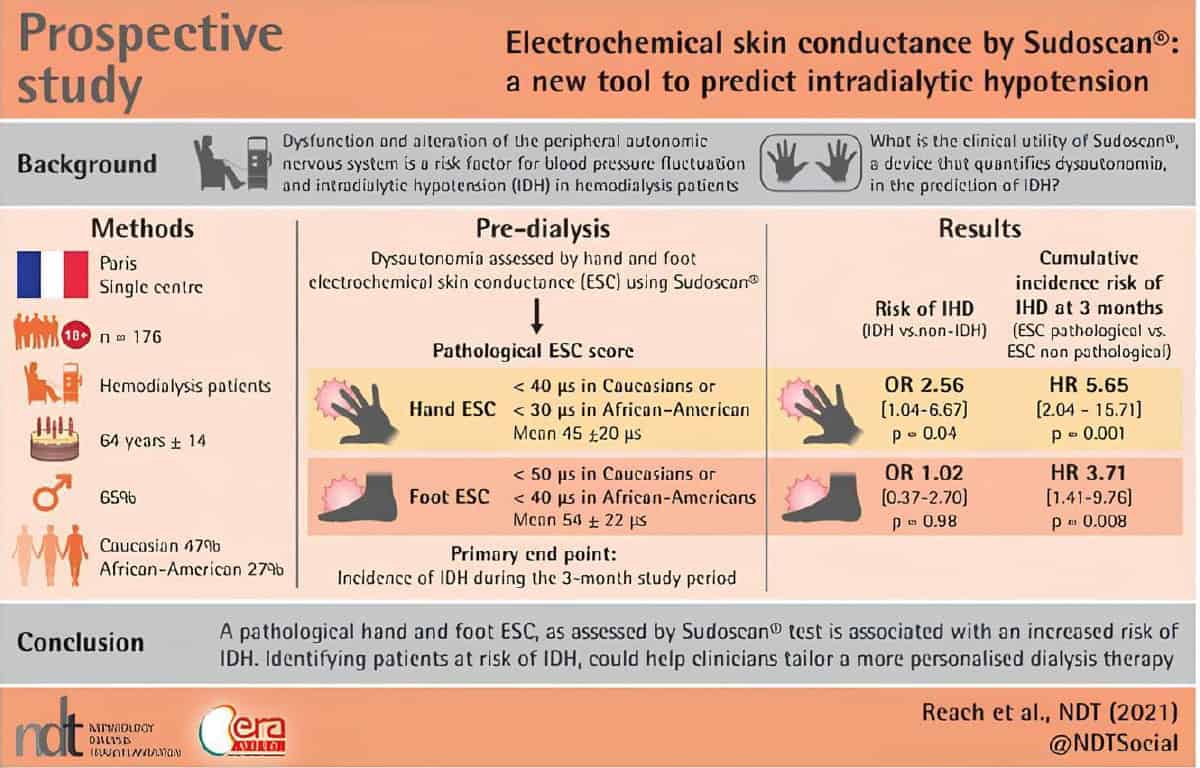
Contexte : L'hypotension intradialytique (HDI) est fréquemment observée chez les patients en hémodialyse (HD) et est liée à plusieurs facteurs de risque, notamment des anomalies cardiaques et du système nerveux autonome. L'étude évalue les bénéfices cliniques du Sudoscan® dans la prédiction de l'HDI en quantifiant la dysautonomie.
Méthodologie : Une étude prospective monocentrique a été menée sur des adultes en HD. La dysautonomie a été évaluée par la conductivité électrochimique de la peau (ESC) à travers les mains et les pieds avec le Sudoscan® avant la séance de dialyse. Le critère principal était l'incidence de l'IDH tout au long de l'étude.
Résultats : Parmi les 176 patients, une proportion significative présentait une pathologie ESC élevée au niveau des mains et des pieds. L'IDH est survenue chez 46 patients. Une pathologie ESC présente avant la dialyse dans les mains est associée à un risque accru d'IDH. Le risque cumulatif d'IDH était significativement plus élevé chez les patients présentant une pathologie ESC au niveau des pieds ou des mains.
3 - Association de la conductance électrochimique de la peau mesurée
par Sudoscan et des résultats cardiovasculaires chez les patients hémodialysés [4].
Contexte : La neuropathie cardiaque autonome (CAN) est une complication fréquente chez les patients souffrant d'insuffisance rénale terminale et un facteur de risque de mort subite. Principalement causée par le diabète sucré, elle est également associée à l'obésité, aux maladies cardiovasculaires et à l'urémie. Le RCA se manifeste par une baisse de la variabilité de la fréquence cardiaque (VFC) et, à un stade avancé, par des symptômes tels que l'hypotension orthostatique et l'ischémie myocardique silencieuse. Les tests permettant d'évaluer le RCA prennent du temps et ne sont pas adaptés à une utilisation clinique de routine.
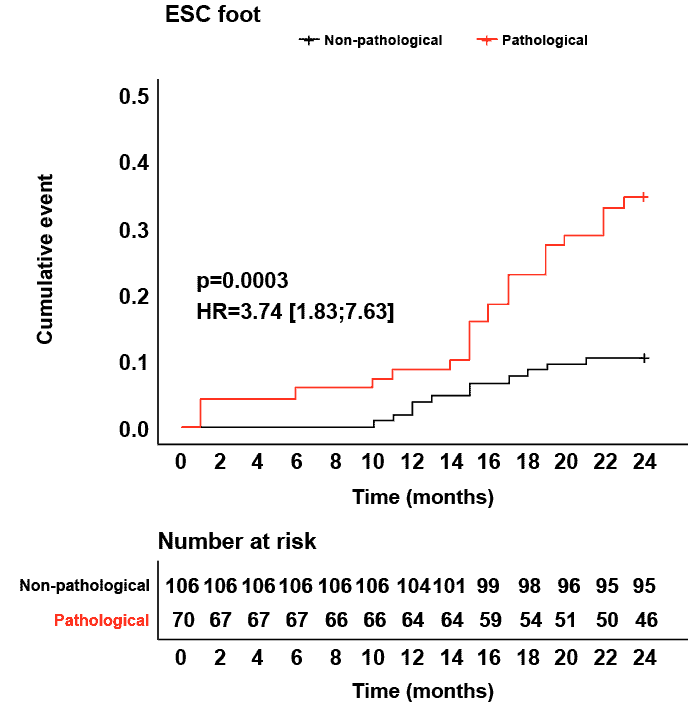
Méthodologie : Cette étude a évalué le Sudoscan, un appareil non invasif mesurant la conductance électrochimique de la peau (ESC) pour prédire les événements cardiovasculaires indésirables majeurs (MACE) chez 176 patients en hémodialyse (HD) pendant 24 mois. Les patients ont été suivis jusqu'à l'apparition des premiers signes de MACE (AVC, infarctus du myocarde) ou de décès.
Résultats : Au cours des 24 mois de l'étude, 41 patients ont connu leur premier événement MACE et 37 sont décédés. Les patients atteints de MACE étaient plus âgés, plus souvent diabétiques et présentaient un niveau plus élevé de fibrillation auriculaire. L'ESC moyen des pieds avant dialyse était significativement plus bas chez les patients avec MACE (47 mS) que chez les patients sans MACE (57 mS). Une pathologie de l'ESC des pieds était associée à un risque accru de décès (HR = 3,74) et de MACE (HR = 2,88). En revanche, aucune association n'a été observée pour le CES des mains.
SUDOSCAN Avantages

Rapide
Pas de préparation du patient
Résultats en 3 minutes
Points de données critiques faciles à lire pour aider les médecins à poser un diagnostic

Sécurisé
Non invasif
Pas de jeûne
Facile à utiliser
Homologations CE et FDA

Précision
Résultats quantitatifs reproductibles
Indépendants des conditions environnementales
Soutenus par des recherches fondées sur des données probantes
150 publications dans des revues à comité de lecture
Références
[1] Levine TD. Neuropathie à petites fibres : Classification des maladies au-delà de la douleur et de la brûlure. J Cent Nerv Syst Dis.2018;10:1179573518771703. Publié 2018 Apr 18.[2] Kharoubi M, Roche F, Bézard M, Hupin D, Silva S, Oghina S, Chalard C, Zaroui A, Galat A, Guendouz S, Canoui-Poitrine F, Hittinger L, Teiger E, Lefaucheur JP, Damy T. Prevalence and prognostic value of autonomic neuropathy assessed by Sudoscan® in transthyretin wild-type cardiac amyloidosis. ESC Heart Fail. 2021 Apr;8(2):1656-1665.
[2] Ozaki R, Cheung KK, Wu E, Kong A, Yang X, Lau E, Brunswick P, Calvet JH, Deslypere JP, Chan JC. A new tool to detect kidney disease in Chinese type 2 diabetes patients : comparison of EZSCAN with standard screening methods. Diabetes Technol Ther. 2011 Sep;13(9):937-43. doi : 10.1089/dia.2011.0023. Epub 2011 Jun 29. PMID : 21714678.
[3] Reach P, Touzot M, Lombardi Y, Maheas C, Sacco E, Fels A, Beaussier H, Ureña-Torres P, Chatellier G, Ridel C, Zuber M. Electrochemical skin conductance by Sudoscan® : a new tool to predict intradialytic hypotension. Nephrol Dial Transplant. 2021 Jul 23;36(8):1511-1518. doi : 10.1093/ndt/gfab183. PMID : 34021358 ; PMCID : PMC8311574.
[4] Touzot M, Reach P, Mobio A, Sacco E, Fels A, Beaussier H, Ureña-Torres P, Chatellier G, Ridel C, Zuber M. Association of Electrochemical Skin Conductance by Sudoscan and Cardiovascular Outcomes in Hemodialysis Patients. Kidney Int Rep. 2022 Sep 16;7(12):2734-2736. doi : 10.1016/j.ekir.2022.09.013. PMID : 36506235 ; PMCID : PMC9727515.





